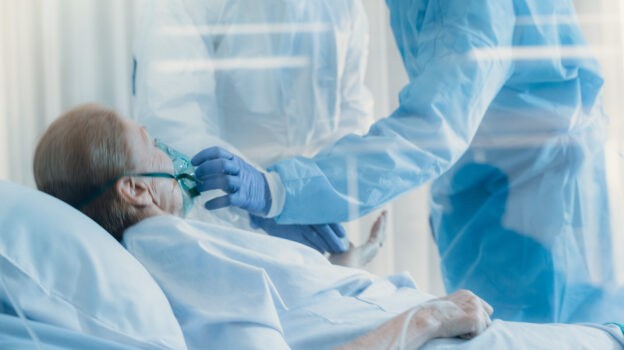
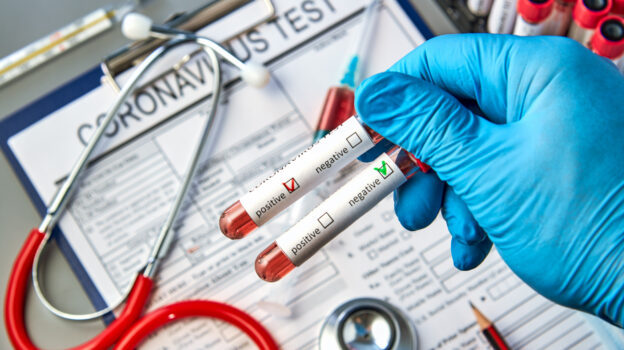
Amerykańska Agencja ds. Żywności i Leków (FDA) zmieniła zezwolenia dotyczące stosowania dodatkowej dawki szczepionki przeciw COVID-19 w sytuacjach wyjątkowych. Trzecią dawkę preparatów firm Pfizer/BioNTech oraz Moderna można podawać pacjentom z obniżoną odpornością.
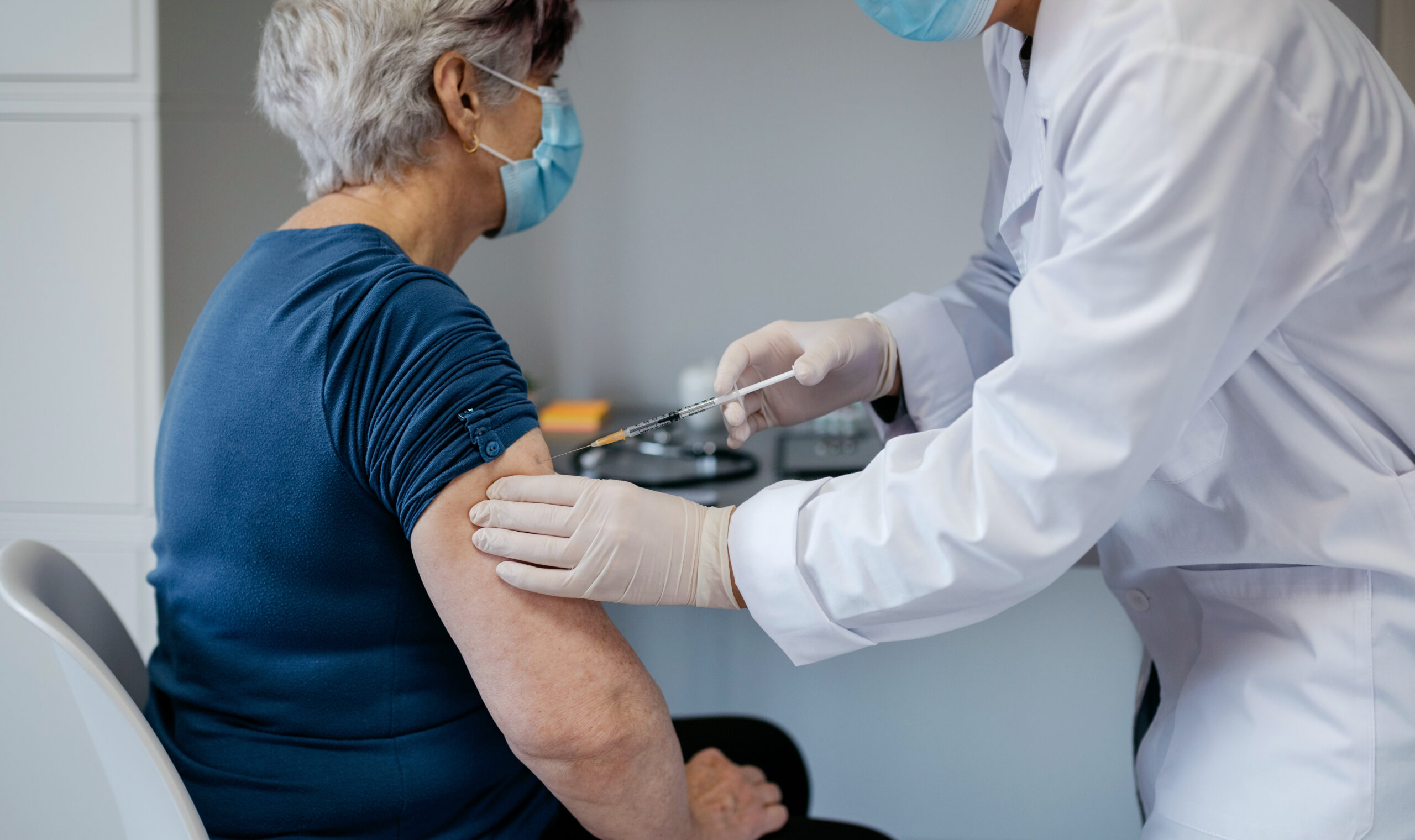
Zalecenia FDA dotyczą w szczególności pacjentów po transplantacji narządu lub ze zdiagnozowanym schorzeniem mającym wpływ na upośledzenie odporności.
– FDA jest świadoma, że osoby z obniżoną odpornością są szczególnie narażone na ciężki przebieg COVID-19. Po dokładnym przeanalizowaniu dostępnych danych FDA ustaliła, że grupa ta może skorzystać z trzeciej dawki szczepionek Pfizer lub Moderna – powiedziała pełniąca obowiązki komisarza FDA dr Janet Woodcock. – Pozostałe osoby, które są w pełni zaszczepione nie potrzebują w tej chwili przypominającej dawki szczepionki przeciw COVID-19. FDA będzie rozważać, czy w przyszłości takie rozwiązanie będzie potrzebne – dodała Woodcock.
Obniżona odporność zwiększa ryzyko ciężkiego przebiegu COVID-19
Jak wyjaśnia FDA w komunikacie na swojej stronie, osoby z obniżoną odpornością mają mniejszą zdolność do zwalczania infekcji i są bardziej podatne na zakażenie COVID-19. Na podstawie badań i danych, Agencja podjęła decyzję, że podanie trzeciej dawki szczepionki może zwiększyć ochronę tych osób.
Jednocześnie organ zaleca, by osoby z obniżoną odpornością, które zachorują na COVID-19, omówiły ze swoim lekarzem opcje leczenia przeciwciałami monoklonalnymi. Terapia ta została zatwierdzona przez FDA do stosowania w nagłych przypadkach – w sytuacjach zagrożenia życia, ryzyka progresji COVID-19 i/lub hospitalizacji. FDA podkreśla, że przeciwciała monoklonalne są dozwolone w leczeniu zapobiegawczym, ale nie zastępują szczepienia.
Pfizer/BioNTech: trzecia dawka szczepionki jest bezpieczna
BioNTech i Pfizer informują, że badania dotyczące podania trzeciej dawki szczepionki, wykazują korzystny profil bezpieczeństwa i silną odpowiedź immunologiczną. Dawka przypominająca wywołała istotnie wyższe miana przeciwciał neutralizujących przeciw SARS-CoV-2, a także przeciw wariantom Beta i Delta, w porównaniu z poziomami obserwowanymi po podaniu dwóch dawek. Według producentów trzecia dawka szczepionki powinna być podana w ciągu 6 do 12 miesięcy po pierwotnym schemacie szczepień.
– Szczepienia to nasz najskuteczniejszy sposób zapobiegania zakażeniu COVID-19 – zwłaszcza ciężkiemu przebiegu choroby i hospitalizacji. Mimo to, przy ciągłym zagrożeniu wariantem Delta i możliwości pojawiania się nowych mutacji w przyszłości, musimy zachować czujność – podkreśla Albert Bourla, CEO Pfizera. – Dane, które do tej pory przeanalizowaliśmy, sugerują, że trzecia dawka naszej szczepionki wywołuje poziom przeciwciał, które znacznie przekraczają poziomy obserwowane po podaniu dwóch dawek – dodaje Bourla.
Dane Pfizera i BioNTechu zostały przekazane FDA. Na ich podstawie organ wydał zalecenie dotyczące stosowania trzeciej dawki szczepionki.
Czy będzie trzecia dawka szczepionki w Polsce?
Jak informuje Michał Dworczyk, szef Kancelarii Prezesa Rady Ministrów, w naszym kraju w sprawie stosowania trzeciej dawki szczepionki przeciw COVID-19 nie ma jeszcze decyzji.
– Trwa dyskusja wśród naukowców, wśród lekarzy o tym, czy nie zastosować trzeciej dawki do wybranych osób, które mają zaniżoną odporność, czy ze względu na inne wskazania, ale tutaj decyzji w tej sprawie jeszcze nie ma. Nie ma też ustalonego takiego jednolitego, międzynarodowego stanowiska i ono jest w tej chwili analizowane – dodaje szef KPRM.
Dworczyk podkreślił, że w grupie seniorów (powyżej 70. roku życia), którzy są najbardziej zagrożeni zakażeniem COVID-19, wyszczepialność sięga 80 proc.
Źródła: FDA, BioNTech, PAP
Przeczytaj także: Ile na sprzedaży szczepionek przeciw COVID-19 zarobiły firmy farmaceutyczne?